Группа Lactobacillus casei (LCG) состоит из близкородственных Lactobacillus casei, Lactobacillus paracasei и Lactobacillus rhamnosus, которые являются одними из наиболее широко исследуемых и применяемых пробиотических видов лактобактерий. Эти три вида были тщательно изучены, классифицированы и реклассифицированы благодаря своим свойствам, способствующим укреплению здоровья.
Благодаря длительному опыту применения этих видов лактобактерий в ферментированных продуктах, они имеют статус GRAS (общепризнаны безопасными) от Управления по контролю за продуктами и лекарствами США (FDA) и находятся в списке QPS (квалифицированной презумпции безопасности) от Европейского агентства по безопасности пищевых продуктов (EFSA). Впервые Lactobacillus casei была предложена как новый вид в 1971 году (Hansen and Lessel).
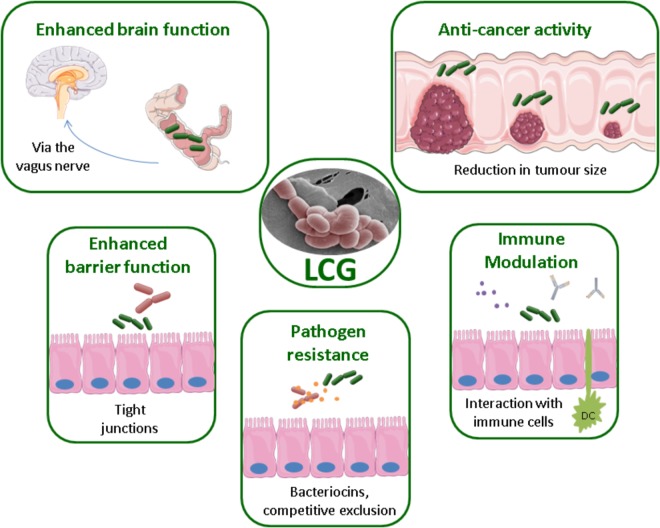
Группа Lactobacillus casei (LCG) содержит множество штаммов с доказанной пробиотической активностью. Существует большой потенциал в области новых функциональных пищевых продуктов и фармабиотиков, полученных из LCG. Способность штаммов L. casei выживать при прохождении через пищеварительную систему и потенциально колонизировать кишечник позволяет некоторым штаммам оказывать прямое воздействие на здоровье человека. Сообщалось о пользе для здоровья, связанной с LCG, при различных состояниях здоровья, от атопического дерматита до рака. См.Рисунок.
Аллергические заболевания
Уровень детской астмы растет, для объяснения этого существует гипотеза гигиены ( Zhang et al.,2016 ). В основе этой теории - предположение, что дети подвергаются меньшему воздействию микробов уже в младенчестве благодаря лучшей гигиене, в дополнение к воздействию антибиотиков, рождению путем кесарева сечения и изменению рациона питания. Эти факторы влияют на развитие микробиоты кишечника и ее иммунную стимуляцию уже в раннем возрасте.
Пробиотики благодаря возможности изменять микробиоту кишечника, показали потенциал для снижения риска развития аллергических заболеваний, например, атопического дерматита. Было показано, что риск развития аллергии у детей снижается до 5-летнего возраста за счет ранней колонизации LCG сразу после рождения как от родителей без аллергических заболеваний, так и с аллергическими заболеваниями. Это может означать, что колонизация LCG защищает от развития аллергического заболевания, несмотря на родительскую аллергию. ( Johansson et al., 2011).
Функция мозга
«Психобиотики» - так можно назвать бактерии, которые при введении в адекватных количествах могут оказывать положительное влияние на психическое здоровье ( Dinan and Cryan, 2017 ). Виды LCG были вовлечены в ряд важных исследований в этой области.
В одном исследовании, посвященном оси мозг-кишечник, штамм L. rhamnosus JB1 показал способность лактобактерий положительно влиять на функцию мозга, продемонстрировал наличие двунаправленной коммуникации между кишечными микробами и мозгом. Введение JB1 напрямую влияет на экспрессию рецепторов ГАМК в головном мозге, что приводит к снижению тревожности и депрессивного поведения у мышей ( Bravo et al., 2011 ). В это исследование были включены здоровые животные в разных лабораториях с одинаковым результатом.
Ожирение
Ожирение - сложный синдром с множеством факторов, влияющих на его возникновение. К ним относятся диета, физическая активность, генетические факторы, обнаружена и зависимость ожирения от состава кишечной микробиоты. Регуляция микробиоты с помощью пробиотиков - метод, который может помочь как в профилактике, так и в лечении ожирения. В исследовании пробиотик L. rhamnosus CGMCC1.3724 вводили мужчинам и женщинам с ожирением в течение 24 недель. Мужчины не показали значительной разницы в потере веса, но женщины, принимавшие пробиотики, значительно похудели. Было обнаружено, что это связано со снижением концентрации лептина в крови на фоне применения пробиотика ( Sanchez et al., 2014).
Рак
Пробиотики были исследованы на предмет их потенциала в качестве дополнительной терапии и микробной терапии рака ( Huang et al., 2016 ; So et al., 2017 ).
Штамм вида L. casei ATCC 393 был исследован на экспериментальной модели рака толстой кишки с использованием линий клеток карциномы толстой кишки мыши и человека ( Tiptiri-Kourpeti et al., 2016 ). Модель in vivo показала уменьшение объема опухоли приблизительно на 80% у мышей, которых кормили живыми L. casei в течение 13 дней. Бактерии прикреплялись к раковым клеткам и снижали жизнеспособность раковых клеток и вызывали апоптотическую гибель клеток. Хотя механизмы до конца не изучены, это дает многообещающие доказательства использования L. casei для лечения рака.
Многочисленные исследования изучали стратегии использования пробиотических штаммов для уменьшения опухоли. L. casei Shirota изучалась в сочетании с пищевыми волокнами на предмет их способности уменьшать рецидив опухолей при колоректальном раке, и первые исследования показали многообещающие результаты ( Ishikawa et al., 2005 ).
Методы лечения онкологических больных могут стать тяжелым бременем для иммунной системы и вызвать побочные эффекты, такие как диарея, которая у человека с ослабленным иммунитетом может оказаться фатальной. Было показано, что пробиотики снижают вероятность радиационно-индуцированной диареи во время лечения рака ( Liu et al., 2017 ). Штамм LGG изучался в качестве дополнительной терапии для лечения рака для снижения частоты и тяжести диареи ( Banna et al., 2017 ). Пациенты, получавшие Lactobacillus rhamnosus GG, реже имели диарею 3 или 4 степени (22 против 37%, P = 0,027), сообщали о меньшем дискомфорте в животе, меньше нуждались в стационарном лечении и реже снижали дозу химиотерапевтических препаратов из-за кишечных проблем.( Osterlund et al., 2007 ).
Диарея
По данным ВОЗ, диарея является второй по значимости причиной смерти детей в возрасте до 5 лет и остается серьезной проблемой, связанной с антибиотиками. Инфекция Clostridium difficile, ассоциированная с антибиотиками, является основной причиной диареи в странах с высоким уровнем доходов во всех возрастных группах. Штаммы LCG были связаны с улучшением симптомов и / или уменьшением продолжительности диареи в многочисленных исследованиях. Способность многих штаммов L. Casei предотвращать диарею, связанную с антибиотиками, обусловлены их способностью поддерживать разнообразие кишечного микробиома людей во время лечения антибиотиками. Это может быть связано с прямым прикреплением штамма к эпителиальным клеткам, что способствует долгосрочной колонизации. Штамм LGG прикрепляется к клеткам слизистой оболочки через фимбрии SpaCBA.
Микробная терапия с помощью бактериальных компонентов
Будущее пробиотиков заключается не только в применении живых бактерий, но и в возможности использования бактериальных компонентов для модуляции иммунной системы. Бактериальные компоненты исследуются на предмет свойств, связанных со здоровьем. В одном исследовании убитый нагреванием штамм L. casei вводили модели колита у мышей. Было показано, что как убитые нагреванием, так и живые штаммы обладают терапевтическим действием на модели воспалительного заболевания кишечника (ВЗК) ( Thakur et al., 2016). Выявленное преимущество является многообещающим, поскольку демонстрирует отсутствие необходимости для штамма выжить при прохождении через кишечник и потенциально может обеспечить более устойчивый эффект, поскольку колонизация бактерий не требуется.
Кислотный шок
Пробиотические бактерии находятся в кислой среде во время транзита через желудочно-кишечный тракт. Группа Lactobacillus casei (LCG) обладают врожденной устойчивостью к кислотному стрессу.
Методы противодействия кислотному стрессу L. Casei включают аргининдезиминазный путь, протонный насос F0F1, особенности клеточной мембраны и восстановление поврежденной ДНК и белков. К примеру, в кислой среде устойчивая к кислотам бактерия L. Casei, демонстрирует более высокий уровень активности АТФазы, чем у чувствительных к кислоте клеток ( Wu et al., 2012a )
Бактерии также адаптируются к изменениям окружающей среды (стрессам), изменяя состав своих мембран ( Zhang and Rock, 2008 ). Было показано, что бактерии изменяют состав жирных кислот своей цитоплазматической мембраны в ответ на кислые условия. Устойчивая к кислоте L. casei Zhang может увеличивать экспрессию белков MurA и MurG, ключевых ферментов синтеза пептидогликана ( Wu et al., 2012a ).
Штаммы группы Lactobacillus casei (LCG), предназначенные для применения в промышленности должны обладать способностью выдерживать ряд стрессовых условий, включая окислительный стресс, осмотический стресс, холодовой стресс, кислотный стресс и долгосрочное хранение. Помимо необходимости выдерживать эти условия при переработке пищевых продуктов, живые штаммы должны быть способны выжить при прохождении через ЖКТ, если они предназначены для целей укрепления здоровья.
Способность LCG к укреплению здоровья была документально подтверждена в исследованиях, свидетельствующих о реальном потенциале их использования при лечении или профилактике различных заболеваний.
Двигаясь вперед, важно, чтобы ученые расшифровали лежащие в основе механизмы действия, чтобы иметь возможность применять эти штаммы или их бактериальные компоненты в качестве новых методов лечения или профилактических вмешательств.
Hill D, Sugrue I, Tobin C, Hill C, Stanton C, Ross RP. The Lactobacillus casei Group: History and Health Related Applications. Front Microbiol. 2018 Sep 10;9:2107. doi: 10.3389/fmicb.2018.02107. PMID: 30298055; PMCID: PMC6160870










